Прогресс лечении диабета 1 типа
Новое исследование ученых из Университета Уппсалы показало многообещающий прогресс в использовании противовоспалительного цитокина для лечения сахарного диабета I типа.
Репрезентативное изображение островков поджелудочной железы мышей с сахарным диабетом, которые не получали ИЛ-35 (слева) и которые получали ИЛ-35 (справа). Коричневый цвет представляет вырабатывающие инсулин бета-клетки. Новое исследование ученых из Университета Уппсалы показало многообещающий прогресс в использовании противовоспалительного цитокина для лечения сахарного диабета I типа. Исследование показало, что введение интерлейкина-35 мышам с сахарным диабетом I типа обращает вспять или излечивает заболевание, поддерживая нормальный уровень глюкозы крови и иммунную толерантность.
Исследование, опубликованное в открытом доступе на сайте журнала Scientific Reports, показало, что введение интерлейкина-35 (белок, вырабатываемый иммунными клетками) мышам с сахарным диабетом I типа обращает вспять или излечивает заболевание, поддерживая нормальный уровень глюкозы крови и иммунную толерантность.
Сахарный диабет I типа – это хроническое заболевание, которое приводит пациентов к зависимости от пожизненных ежедневных инъекций инсулина.
В Швеции каждый день диагностируется примерно 2 новых случая этого заболевания. Инсулин – это гормон. Который вырабатывается бета-клетками поджелудочной железы. Инсулин необходим для предотвращения вредного повышения уровня глюкозы крови.
Точная причина сахарного диабета I типа все еще неизвестна, однако он считается аутоиммунным заболеванием, которое возникает, когда наша собственная иммунная система ошибочно нападает и уничтожает здоровые клетки.
Вероятно, при сахарном диабете I типа инфекционный процесс и/или другие неизвестные факторы запускают нападение иммунных клеток, которое, в конечном итоге, приводит к недостаточному производству инсулина.
В новом исследовании доктор Кайлаш Сингх, аспирант научно-исследовательской группы профессора Стеллана Сэндлера в отделении медицинской клеточной биологии в Университете Уппсалы, изучил действия иммунных регуляторных Т-клеток в мышиных моделях сахарного диабета I типа.
Исследование показало, что иммунные регуляторные Т-клетки в условиях сахарного диабета I типа изменяют свои функции, вырабатывая провоспалительные разрушающие белки вместо защитных противовоспалительных белков, таких как интерлейкин-35 (ИЛ-35).
«Это подтверждает то, что хорошие парни становятся плохими в начале развития сахарного диабета I типа, и, таким образом, наши иммунные клетки разрушают бета-клетки», – говорит доктор Кайлаш Сингх.
Кроме того, у пациентов с сахарным диабетом I типа наблюдалась более низкая концентрация ИЛ-35, в сравнении со здоровыми людьми. Эти данные могут подтверждать то, что ИЛ-35 может играть очень важную роль в развитии сахарного диабета I типа у людей.
Кроме этого, исследователи обнаружили новый механизм, который объясняет, как иммунные регуляторные Т-клетки изменяют свое предназначение в условиях сахарного диабета I типа.
Научно-исследовательская группа профессора Сэндлера протестировала, может ли ИЛ-35 также подавлять развитие сахарного диабета I типа и обращать вспять уже имеющийся диабет.
Для того, чтобы вызвать сахарный диабет I типа у мышей, ученые вводили им химическое соединение под названием стрептозоцин. У этих мышей развивались признаки сахарного диабета I типа и высокие уровни глюкозы крови, подобно этому заболеванию у людей.
Инъекции ИЛ-35, проведенные после индукции заболевания, предупреждали развитие сахарного диабета I типа. Поразительно было то, что инъекции ИЛ-35 мышам, которые были диабетическими в течение двух дней подряд, нормализовали уровни глюкозы крови.
Научно-исследовательская группа также успешно изучила ИЛ-35 в другой модели сахарного диабета I типа, так называемых NOD-мышах (non-obese diabetic mouse). Прерывание лечения ИЛ-35 не приводило к возвращению сахарного диабета в любой из мышиных моделей.
Результаты поощряют проведение дальнейших исследований по использованию ИЛ-35 для лечения сахарного диабета I типа и предлагают новые идеи о том, почему иммунные регуляторные Т-клетки не противодействуют развитию этого заболевания.
«Чтобы улучшить наши знания, мы впервые показали, что ИЛ-35 может обратить вспять уже существующий сахарный диабет I типа в двух разных мышиных моделях, и что концентрация конкретного цитокина ниже у пациентов с этим заболеванием, в сравнении со здоровыми людьми.
Также мы предоставили идеи о новом механизме – как иммунные регуляторные Т-клетки изменяют свое предназначение при аутоиммунных заболеваниях», – сказал доктор Кайлаш Сингх.
Дата публикации: 2015-07-31
Последнее изменение: 2020-01-31
Дорогие друзья. Статья не является медицинским советом и не может служить заменой консультации с врачом.
Источник
Ññûëêà íà íîâîñòü: https://www.mk.ru/science/article/2013/07/03/878571-novaya-vaktsina-zastavlyaet-organizm-diabetikov-vyirabatyivat-insulin-samostoyatelno.html
Ñîáñòâåííî ñàìà íîâîñòü.
Øïðèöû â óéäóò â ïðîøëîå — íîâàÿ ÄÍÊ-âàêöèíà áûëà óñïåøíî èñïûòàíà íà ÷åëîâåêå
Áëàãîäàðÿ ðàçðàáîòêå íîâîãî ìåòîäà ëå÷åíèÿ ëþäè, êîòîðûå ñòðàäàþò îò ñàõàðíîãî äèàáåòà ïåðâîãî òèïà, â ñêîðîì âðåìåíè ñìîãóò çàáûòü î øïðèöàõ è ïîñòîÿííûõ èíúåêöèÿõ èíñóëèíà.  íàñòîÿùåå âðåìÿ äîêòîð Ëîóðåíñ Øòåéíìàí èç Ñòýíôîðäñêîãî óíèâåðñèòåòà ñîîáùèë, ÷òî íîâûé ìåòîä ëå÷åíèÿ ñàõàðíîãî äèàáåòà ïåðâîãî òèïà áûë óñïåøíî èñïûòàí íà ÷åëîâåêå è ìîæåò íàéòè øèðîêîå ïðèìåíåíèå ïðè ëå÷åíèè äàííîé áîëåçíè â îáîçðèìîì áóäóùåì.
äèàáåò äèàáåò ïåðâîãî òèïà èíñóëèí ëîóðåíñ øòåéíìàí âàêöèíà lawrence steinman íåâðîëîãèÿ
Ëîóðåíñ Øòåéíìàí (Lawrence Steinman), M.D./Stanford University
Òàê íàçûâàåìàÿ «ðåâåðñèðîâàííàÿ âàêöèíà» ðàáîòàåò ïóòåì ïîäàâëåíèÿ èììóííîé ñèñòåìû íà óðîâíå ÄÍÊ, ÷òî â ñâîþ î÷åðåäü ñòèìóëèðóåò ïðîèçâîäñòâî èíñóëèíà. Ðàçðàáîòêà Ñòýíôîðäñêîãî óíèâåðñèòåòà ìîæåò ñòàòü ïåðâîé ÄÍÊ-âàêöèíîé â ìèðå, êîòîðóþ ìîæíî áóäåò ïðèìåíÿòü äëÿ ëå÷åíèÿ ëþäåé.
«Äàííàÿ âàêöèíà èñïîëüçóåò ñîâåðøåííî äðóãîé ïîäõîä. Îíà áëîêèðóåò ñïåöèôè÷åñêèé îòâåò èììóííîé ñèñòåìû, à íå ñîçäàåò ñïåöèôè÷åñêèå èììóííûå ðåàêöèè, êàê îáû÷íûå âàêöèíû ïðîòèâ ãðèïïà èëè ïîëèîìèåëèòà», ãîâîðèò Ëîóðåíñ Øòåéíìàí.
Âàêöèíà áûëà ïðîòåñòèðîâàíà íà ãðóïïå èç 80 äîáðîâîëüöåâ. Èññëåäîâàíèÿ ïðîâîäèëèñü íà ïðîòÿæåíèè äâóõ ëåò è ïîêàçàëè, ÷òî ó ïàöèåíòîâ, êîòîðûå ïîëó÷èëè ëå÷åíèå ïî íîâîé ìåòîäèêå, íàáëþäàëîñü ñíèæåíèå àêòèâíîñòè êëåòîê, ðàçðóøàþùèõ èíñóëèí â èììóííîé ñèñòåìå. Ïðè ýòîì íèêàêèõ ïîáî÷íûõ ïîñëåäñòâèé ïîñëå ïðèåìà âàêöèíû çàôèêñèðîâàíî íå áûëî.
Êàê ÿñíî èç íàçâàíèÿ, òåðàïåâòè÷åñêàÿ âàêöèíà ïðåäíàçíà÷åíà íå äëÿ ïðîôèëàêòèêè áîëåçíè, à äëÿ ëå÷åíèÿ óæå èìåþùåãîñÿ çàáîëåâàíèÿ.
Ó÷åíûå, îïðåäåëèâ êàêèå èìåííî ðàçíîâèäíîñòè ëåéêîöèòîâ, ãëàâíûõ «âîèíîâ» èììóííîé ñèñòåìû, àòàêóþò ïîäæåëóäî÷íîþ æåëåçó, ñîçäàëè ïðåïàðàò, êîòîðûé ñíèæàåò â êðîâè êîëè÷åñòâî èìåííî ýòèõ êëåòîê, íå âëèÿÿ íà îñòàëüíûå êîìïîíåíòû èììóíèòåòà.
Ó÷àñòíèêè èñïûòàíèé îäèí ðàç â íåäåëþ íà ïðîòÿæåíèè 3-õ ìåñÿöåâ ïîëó÷àëè èíúåêöèè íîâîé âàêöèíû. Ïàðàëëåëüíî èì ïðîäîëæàëè ââîäèòü èíñóëèí.
 êîíòðîëüíîé ãðóïïå áîëüíûå íà ôîíå èíúåêöèé èíñóëèíà ïîëó÷àëè âìåñòî âàêöèíû ïðåïàðàò ïëàöåáî.
Ñîçäàòåëè âàêöèíû ñîîáùàþò, ÷òî â ýêñïåðèìåíòàëüíîé ãðóïïå, ïîëó÷àâøåé íîâûé ïðåïàðàò, íàáëþäàëîñü çíà÷èòåëüíîå óëó÷øåíèå ðàáîòû áåòà-êëåòîê, êîòîðûå ïîñòåïåííî âîññòàíàâëèâàëè ñïîñîáíîñòü âûðàáàòûâàòü èíñóëèí.
«Ìû áëèçêè ê âîïëîùåíèþ â æèçíü ìå÷òû ëþáîãî âðà÷à-èììóíîëîãà: ìû íàó÷èëèñü âûáîðî÷íî «âûêëþ÷àòü» äåôåêòíûé êîìïîíåíò èììóííîé ñèñòåìû, íå âëèÿÿ íà åå ðàáîòó â öåëîì», êîììåíòèðóåò îäèí èç ñîàâòîðîâ ýòîãî îòêðûòèÿ ïðîôåññîð Ëîóðåíñ Øòåéíìýí (Lawrence Steinman).
Äèàáåò 1-ãî òèïà ñ÷èòàåòñÿ áîëåå òÿæåëûì çàáîëåâàíèåì, ÷åì åãî «ñîáðàò» äèàáåò 2-ãî òèïà.
Ñàìî ñëîâî äèàáåò — ïðîèçâîäíîå ãðå÷åñêîãî ñëîâà «äèàáàéíî», ÷òî çíà÷èò «ïðîõîæó ÷åðåç ÷òî-íèáóäü, ñêâîçü», «ïðîòåêàþ». Àíòè÷íûé âðà÷ Àðåòåóñ Êàïïàäîêèéñêèé (30 90 ã. í. ý.) íàáëþäàë ó ïàöèåíòîâ ïîëèóðèþ, êîòîðóþ ñâÿçûâàë ñ òåì, ÷òî æèäêîñòè, ïîñòóïàþùèå â îðãàíèçì, ïðîòåêàþò ÷åðåç íåãî è âûäåëÿþòñÿ â íåèçìåí¸ííîì âèäå.  1600 ã. í. ý. ê ñëîâó äèàáåò äîáàâèëè mellitus (îò ëàò. mel ì¸ä) äëÿ îáîçíà÷åíèÿ äèàáåòà ñî ñëàäêèì âêóñîì ìî÷è ñàõàðíîãî äèàáåòà.
Ñèíäðîì íåñàõàðíîãî äèàáåòà áûë èçâåñòåí åù¸ â ãëóáîêîé äðåâíîñòè, íî äî XVII âåêà ðàçëè÷èé ìåæäó ñàõàðíûì è íåñàõàðíûì äèàáåòîì íå çíàëè.  XIX íà÷àëå XX âåêà ïîÿâèëèñü îáñòîÿòåëüíûå ðàáîòû ïî íåñàõàðíîìó äèàáåòó, óñòàíîâëåíà ñâÿçü ñèíäðîìà ñ ïàòîëîãèåé öåíòðàëüíîé íåðâíîé ñèñòåìû è çàäíåé äîëè ãèïîôèçà.  êëèíè÷åñêèõ îïèñàíèÿõ ïîä òåðìèíîì «äèàáåò» ÷àùå ïîäðàçóìåâàþò æàæäó è ìî÷åèçíóðåíèå (ñàõàðíûé è íåñàõàðíûé äèàáåò), îäíàêî, åñòü è «ïðîõîæó ñêâîçü» ôîñôàò-äèàáåò, ïî÷å÷íûé äèàáåò (îáóñëîâëåííûé íèçêèì ïîðîãîì äëÿ ãëþêîçû, íå ñîïðîâîæäàåòñÿ ìî÷åèçíóðåíèåì) è òàê äàëåå.
Íåïîñðåäñòâåííî ñàõàðíûé äèàáåò ïåðâîãî òèïà çàáîëåâàíèå, îñíîâíûì äèàãíîñòè÷åñêèì ïðèçíàêîì êîòîðîãî ÿâëÿåòñÿ õðîíè÷åñêàÿ ãèïåðãëèêåìèÿ ïîâûøåííûé óðîâåíü ñàõàðà â êðîâè, ïîëèóðèÿ, êàê ñëåäñòâèå ýòîãî æàæäà; ïîòåðÿ âåñà; ÷ðåçìåðíûé àïïåòèò, ëèáî îòñóòñòâèå òàêîâîãî; ïëîõîå ñàìî÷óâñòâèå. Ñàõàðíûé äèàáåò âîçíèêàåò ïðè ðàçëè÷íûõ çàáîëåâàíèÿõ, âåäóùèõ ê ñíèæåíèþ ñèíòåçà è ñåêðåöèè èíñóëèíà. Ðîëü íàñëåäñòâåííîãî ôàêòîðà èññëåäóåòñÿ.
Äèàáåò 1 òèïà ìîæåò ðàçâèòüñÿ â ëþáîì âîçðàñòå, îäíàêî íàèáîëåå ÷àñòî çàáîëåâàþò ëèöà ìîëîäîãî âîçðàñòà (äåòè, ïîäðîñòêè, âçðîñëûå ëþäè ìîëîæå 30 ëåò).  îñíîâå ïàòîãåíåòè÷åñêîãî ìåõàíèçìà ðàçâèòèÿ äèàáåòà 1 òèïà ëåæèò íåäîñòàòî÷íîñòü âûðàáîòêè èíñóëèíà ýíäîêðèííûìè êëåòêàìè (-êëåòêè îñòðîâêîâ Ëàíãåðãàíñà ïîäæåëóäî÷íîé æåëåçû), âûçâàííîå èõ ðàçðóøåíèåì ïîä âëèÿíèåì òåõ èëè èíûõ ïàòîãåííûõ ôàêòîðîâ (âèðóñíàÿ èíôåêöèÿ, ñòðåññ, àóòîèììóííûå çàáîëåâàíèÿ è äðóãèå).
Äèàáåò 1 òèïà ñîñòàâëÿåò 1015% âñåõ ñëó÷àåâ äèàáåòà, ÷àùå ðàçâèâàåòñÿ â äåòñêîì èëè ïîäðîñòêîâîì ïåðèîäå. Îñíîâíûì ìåòîäîì ëå÷åíèÿ ÿâëÿþòñÿ èíúåêöèè èíñóëèíà, íîðìàëèçóþùèå îáìåí âåùåñòâ ïàöèåíòà.  îòñóòñòâèå ëå÷åíèÿ äèàáåò 1 òèïà áûñòðî ïðîãðåññèðóåò è ïðèâîäèò ê âîçíèêíîâåíèþ òÿæ¸ëûõ îñëîæíåíèé, òàêèõ êàê êåòîàöèäîç è äèàáåòè÷åñêàÿ êîìà, çàêàí÷èâàþùèåñÿ ñìåðòüþ áîëüíîãî.
à òåïåðü êðàòêîå äîáàâëåíèå. ß ñàì áîëåþ äèàáåòîì 16 ëåò. äëÿ ìåíÿ â æèçíè ýòî ïðèíåñëî ìíîãî ïðîáëåì, õîòÿ áûëà â ýòîì è ïîëüçà. Áåç ýòîé áîëåçíè ÿ áû íå ñòàë òåì, êòî ÿ åñòü. ÿ áû íå íàó÷èëñÿ òàêîìó ñàìîêîíòðîëþ, íå ïîâçðîñëåë áû ðàíüøå ñâåðñòíèêîâ… äà ìíîãî ÷åãî. Íîÿ ìîëþñü, ÷òîáû ôàðìàöåâòû, êîòîðûå äåëàþò íà ýòîé áåäå îãðîìíûå ñîñòîÿíèÿ íå çàãóáèëè ýòî äåëî. âñåì áîëüíûì æåëàþ äîæèòü äî ÷óäåñíîãî ìîìåíòà, êîãäà ýòà áîëåçíü îòñòóïèò. âñåì ïå÷åíåê ðåáÿò))
Источник
Сахарный диабет — одна из самых прогрессирующих болезней человечества. Введение инсулина для человека с сахарным диабетом 1 типа пока ничем не заменимая процедура. Но благодаря новым методам лечения, возможно, в скором времени удастся освободить людей из плена этой тяжелой болезни.

Новейшие исследования показали, что введение минимального числа заключенных в микрокапсулы клеток поджелудочной железы нормализовало уровень глюкозы в крови подопытных животных на 17 недель и более. Сахарный диабет без инсулина (без его самостоятельного введения) становится достижимой реальностью.
Число людей, живущих с сахарным диабетом, уже 425 миллионов. К 2045 году таких людей в мире станет более 630 миллионов.
Если человек с сахарным диабетом не борется с ним — не следит за состоянием уровня глюкозы в крови, не соблюдает диету и норму физической нагрузки, не использует необходимые лекарства, а при необходимости — инсулин, то его ждут крайне тяжелые осложнения, лишение нормального образа жизни и ранняя смерть.
Наиболее тяжелая форма болезни — сахарный диабет 1 типа. В этом случае у человека погибают бета-клетки в его поджелудочной железе и его организм теряет возможность производить собственный гормон инсулин. Без инсулина клетки организма не в состоянии нормально существовать, в частности, получать глюкозу из крови — в результате человек погибает.
Сахарный диабет I типа составляет до 10% всех случаев диабета.
Среди детей наиболее распространенным является именно сахарный диабет 1 типа. Всего на данный момент им страдают более 1 миллиона детей по всему миру.
Единственным опробованным, массовым и надежным способом жизни с сахарным диабетом 1 типа на сегодняшний день является инсулинотерапия. Только постоянный мониторинг уровня сахара в крови (с помощью глюкометра или систем постоянного мониторинга, вроде Freestyle Libre или Dexcom ), постоянные инъекции инсулина с помощью шприц-ручек или инсулиновых помп и учет съеденного — дают шанс человеку на полноценную жизнь.
Если человек с сахарным диабетом успешно осуществляет самоконтроль и ему удается проводить успешную инсулинотерапию, то его качество жизни ничем не отличается от обычной, и он сможет реализоваться наравне со всеми — чему свидетельствуют многие очень успешные люди — политики, ученые, спортсмены и актеры с сахарным диабетом.
Однако инсулинотерапия не восстанавливает физиологическую саморегуляцию, требует постоянных усилий со стороны человека и его близких и сохраняет постоянный риск опасных состояний — гипогликемии и сопутствующих сахарному диабету осложнений.
Уже несколько десятилетий ведется поиск альтернативных решений проблемы сахарного диабета 1 типа. Одно из них — создание «искусственной поджелудочной железы», которая самостоятельно контролирует уровень сахара в крови и вводит необходимые дозы инсулина (1,2).
Второй путь — пересадка донорской поджелудочной железы или её фрагментов; пересадка островков поджелудочной железы (с бета-клетками) от человека или животных а также попытки искусственного выращивания инсулин-продуцирующих клеток из стволовых клеток для их последующего ввода в организм.
Но этот путь до сих пор сталкивался с существенными сложностями. Пересадки от человека — из-за крайне малого числа донорского материала по сравнению с требуемым, высокой стоимости и большого числа иммунных реакций организма на пересажанный материал.
Пересадки островков поджелудочной железы от животных также сталкиваются с большим числом трудностей. Главные из которых: нефункционирование должным образом пересаженных клеток, иммунный ответ организма и опасность заражения человека (и человеческой популяции в целом) болезнями животных-доноров.
В частности, чтобы сохранить эффективность пересаженных клеток, человеку приходится принимать сильные иммуннодепрессанты, тем самым существенно снижая собственную защитную систему и подвергая свою жизнь большому риску.
Крайне недостаточное число материала для пересадки от человека (донорами могут быть только погибшие люди) и серьезная (к счастью, пока гипотетическая) опасность заразить человечество зооинфекцией в случае пересадки клеток от животных стимулируют разработку технологий создания тканеинженерных конструкций, замещающих работу островков поджелудочной железы. Клетки, которые должны выполнять функцию погибших бета-клеток человека, либо выделяются из донорского материала, либо выращиваются из различного типа стволовых клеток и «закрепляются» в специальных биокаркасах.
К сожалению, попытки выращивания работающих островковых клеток из различного типа стволовых клеток пока не привели к тому уровню успешности, когда полученные клетки можно было бы использовать для лечения сахарного диабета. Биоинженерные же работы с клетками доноров вполне успешны.
Например, решением части проблем клеточной трансплантации является технология заключения островков поджелудочной железы в микрокапсулы, которые и вводятся больному сахарным диабетом 1 типа. Технология микрокапсулирования помогает изолировать клетки островков поджелудочной железы доноров от иммунной системы пациента. При этом сами клетки должны как можно дольше сохранять жизнедеятельность (осуществлять свободный обмен питательными веществами и кислородом) и эффективно выполнять свою основную функцию — производить инсулин в ответ на повышение уровня глюкозы в крови.
Современные технологии позволяют производить такие микрокапсулы из биосовместимых и нетоксичных материалов. Различные группы ученых во многих странах пытаются усовершенствовать данный метод.
Одна из недавно решенных задач – это уменьшение числа вводимых микрокапсул. Дело в том, что ранее, в процессе микрокапсулирования островков поджелудочной железы, большая часть микрокапсул оставалась пустыми. Из-за этого значительно увеличился объем имплантируемого материала, что сильно увеличивало иммунную реакцию после имплантации.
Для разделения микрокапсул использовались магнитные наночастицы и созданный с помощью 3D-печати чип с микроканалами, который и разделял полученные ранее микрокапсулы на пустые и те, в которых находились островки поджелудочной железы. В результате общий объем имплантата снизился почти на 80%.
Очищенные имплантаты вводились подкожно крысам с сахарным диабетом 1 типа — в результате в течение более 17 недель уровень глюкозы в крови животных восстанавливался до нормогликемии (<200 мг / дл).
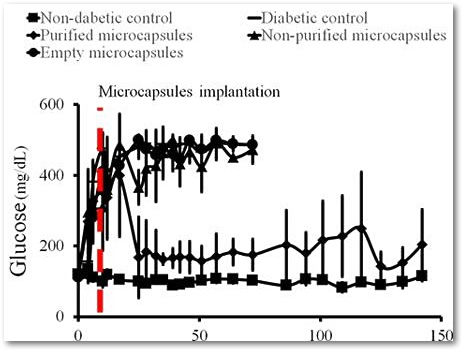
Уровень глюкозы в крови у подопытных крыс. Вверху: графики животных с введенными пустыми микрокапсулами (большие точки); с несортированными микрокапсулами (треугольники). Внизу: график животных с отобранными микрокапсулами (маленькие точки) и контрольный график уровня глюкозы у животных без сахарного диабета (квадраты).
Этот и подобные эксперименты дарят надежду миллионам больным сахарным диабетом на то, что в скором времени удастся совершить прорыв лечении одной из самых массовых болезней человечества.
Пока же больные сахарным диабетом 1 типа должны особо тщательно соблюдать процедуры инсулинотерапии, чтобы сохранить своё здоровье до массового внедрения новых технологий.
Поделиться / сохранить у себя:
ТЕМЫ: Биология Здоровье Человек Болезни Диета Продолжительность жизни
ЧИТАЙТЕ ТАКЖЕ:
Источник
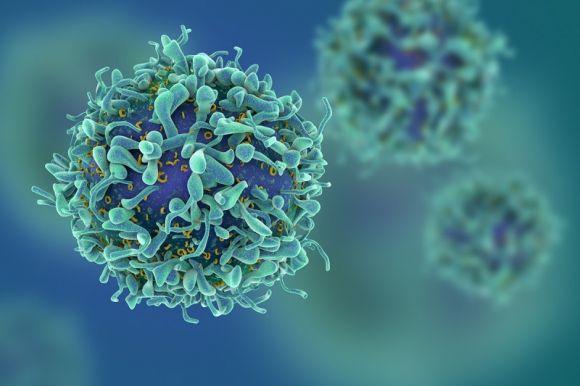
Достижения в биоинженерии Т-клеток для лечения рака открывают возможности в иммунотерапии аутоиммунных заболеваний, в том числе диабета 1 типа. Сейчас исследователи работают над видами лечения, способными перепрограммировать Т-клетки с целью «отключения» иммунной реакции, что может быть многообещающим при лечении сахарного диабета 1 типа, а также других заболеваний, в основе которых лежит атака Т-клетками здоровых тканей и органов человека.


- Автор:
Команда журнала «СахарОК»
- access_time
При лечении раковых заболеваний основной задачей является стимуляция иммунной системы к поиску и уничтожению опухолевых клеток; в терапии аутоиммунных заболеваний требуется программирование собственных Т-клеток организма таким образом, чтобы они снизили активность иммунной системы.
Включение техник преобразования генов обеспечило прогресс в изменении поведения Т-клеток, необходимого для того, чтобы заставить отступить диабет 1 типа. В новом исследовании ученые применят недавние разработки в области иммунотерапии Т-клетками, впервые испытав их на людях.
Первоначально ученым удалось модифицировать Т-клетки человека, задача которых состояла бы в регуляции иммунного ответа организмом. Эти регуляторные Т-клетки (Т-супрессоры) показали свою способность отключать «опасные» эффекторные Т-клетки как в лабораторных условиях, так и в испытаниях на животных. Параллельно ученые смогли изолировать Т-клетки, распознающие специфическую «антигенную» мишень, и преобразовать антиген-специфические эффекторные клетки в регуляторные Т-клетки.

Новые исследования направлены на выделение опасных эффекторных Т-клеток, которые ввиду нарушения своей функции при диабете 1 типа атакуют поджелудочную железу, препятствуя продукции инсулина, и превращение их в регуляторные Т-клетки. Эти регуляторные Т-клетки, модифицированные с помощью генной инженерии, по возвращении в организм диабетика смогут остановить эффекторные Т-клетки, разрушающие инсулин-продуцирующие клетки.
Преимуществом использования регуляторных Т-клеток в лечении диабета является возможность сосредоточить эффект иммуносупрессии на определенном органе, не вовлекая при этом всю иммунную систему. Целью является отправка перепрограммированных Т-клеток непосредственно в поджелудочную железу, и предотвращение атаки на нее, не задействовав здоровые иммунные клетки.
Существует надежда, что новый вид лечения может заменить инсулинотерапию. Введение модифицированных Т-клеток в организм человека, у которых начинает развиваться диабет 1 типа, способно избавить от пожизненной необходимости введения инсулина. Диабет 1 типа как правило развивается в детском возрасте, требуя от пациента тщательного измерения дозы вводимого инсулина каждый день, поскольку инсулин – единственный вид лечения диабета 1 типа на сегодняшний день, будь то инъекции или инсулиновая помпа. Диабет требует полного изменения стиля жизни, поскольку плохой контроль уровня сахара приводит к перепадам уровня глюкозы в крови и, как следствие, повреждению органов и систем.
Кроме диабета, иммунотерапия Т-клетками в перспективе может найти свое применение в лечении ВИЧ инфекции, опухолевых заболеваний, реакций отторжения трансплантатов, а также генетических заболеваний. Ученые воодушевлены первыми результатами и продолжают активно работать в этом направлении.
Источник
